Investigadores del Instituto Catalán de Nanociencia y Nanotecnología y otros centros europeos fabricarán un dispositivo biosensor para analizar en menos de 30 minutos la presencia del nuevo coronavirus en muestras de pacientes. El proyecto, denominado CoNVat, toma lo mejor de los sistemas de diagnóstico actuales, como las pruebas PCR y los test rápidos. FOTO: El proyecto europeo CoNVat lo lidera la investigadora Laura M. Lechuga del CSIC desde el Instituto Catalán de Nanociencia y Nanotecnología. / ICN2
El proyecto europeo CoNVat, liderado desde el Instituto Catalán de Nanociencia y Nanotecnología (ICN2) por la investigadora Laura M. Lechuga del CSIC, diseñará un nuevo sistema de diagnóstico de la COVID-19 que recoge lo mejor de las diferentes técnicas existentes.
A través de una plataforma biosensora basada en nanotecnología óptica, pretende proporcionar un diagnóstico de la enfermedad provocada por el coronavirus SARS-CoV-2 de manera precisa, rápida y sin necesidad de instrumentación compleja.
Una sencilla plataforma biosensora basada en nanotecnología óptica proporcionará un diagnóstico preciso de la COVID-19 en menos de 30 minutos
En este proyecto, financiado con más de dos millones de euros por la Unión Europea a través de una convocatoria rápida frente a la COVID-19, en el marco del Horizonte 2020, colaboran la Universidad de Barcelona, la Universidad Aix-Marsella (Francia) y el Instituto Nacional de Enfermedades Infecciosas (Italia).
La tecnología sensora consiste en un microchip con guías de onda interferométricas, que actualmente ofrecen la más alta sensibilidad para el diagnóstico de biomarcadores clínicos. Estos microchips permiten la detección y cuantificación de moléculas o virus en un solo paso, sin necesidad de amplificación previa o posterior, por lo que el análisis completo puede realizarse en menos de 30 minutos.
Unión del virus e identificación de su ARN
Por un lado, monitorizará la unión del virus al sensor en tiempo real mediante anticuerpos específicos anclados en la superficie sensora (que se asocian a los antígenos o proteínas del patógeno), lo que permitirá dar una respuesta diagnóstica rápida y la cuantificación de la carga viral a partir de muestras de fluido nasofaríngeo, saliva o cualquier otro fluido de interés.
Por otra parte, identificará el ARN viral mediante sondas de ADN complementarias. Este ensayo genómico no necesita de procesos de amplificación por PCR y permite realizar diversos tests simultáneos en el mismo chip para distinguir qué tipo de virus contiene la muestra.
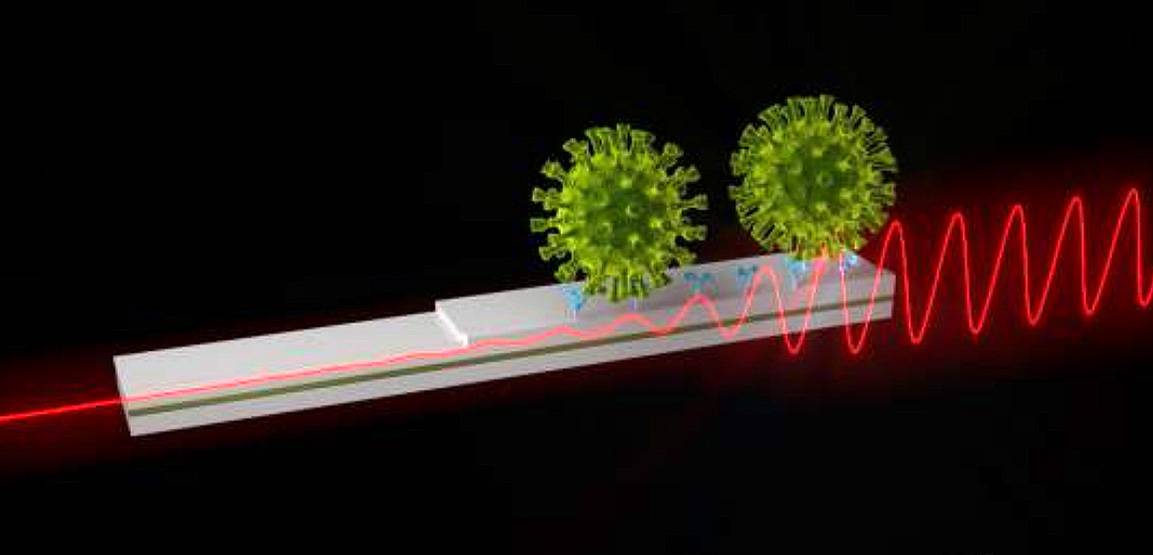
Ilustración del biosensor nanofotónico para la detección de SARS-CoV-2. / ICN2
Junto al Hospital de la Vall d'Hebrón en Barcelona y la Universidad de Aix-Marsella, el ICN2 también ha empezado a estudiar las posibilidades de adaptar la tecnología sensora para el análisis serológico (detección de anticuerpos en suero sanguíneo).
Durante el primer año del proyecto CoNVat se fabricará el biosensor y se llevará a pacientes reales, y en el segundo se realizarán monitorizaciones en el laboratorio de animales que transportan el virus
En resumen, la idea es desarrollar el dispositivo biosensor de análisis muy rápido del coronavirus completo en las muestras de pacientes. Y el sistema permitirá diferenciarlo de otros virus, como el de la gripe, y valorar su carga viral.
Durante el primer año del proyecto se fabricará el biosensor y se llevará a pacientes reales, y en el segundo se realizarán monitorizaciones en el laboratorio de animales que transportan el virus.
Este sistema busca superar algunas de las prestaciones de las herramientas actuales (PCR y test rápidos de antígenos y serológicos), tomando lo mejor de cada estrategia y tratando de descartar sus desventajas.
De hecho, en paralelo a la propuesta del biosensor, el Grupo de Nanobiosensores y Aplicaciones Bioanalíticas del ICN2 ha elaborado un estudio que revisa los diferentes métodos de diagnóstico disponibles para la COVID-19.
Este informe proporciona una visión general tanto de las técnicas convencionales usadas en laboratorios clínicos como de nuevos sistemas en fases de desarrollo y comercialización que pueden ser útiles para una monitorización de la población y la detección rápida del virus SARS-CoV-2 y la enfermedad COVID-19.
Tres sistemas para diagnosticar la COVID-19
Según recuerda el informe del ICN2, los métodos de detección de virus respiratorios se pueden clasificar en tres estrategias diferenciadas:
1. Detección del material genético (ARN) del virus mediante la PCR
Esta es la detección más compleja, pero la que se desarrolla más rápido gracias a las importantes inversiones en investigación de genómica que se hicieron para obtener el genoma humano en los años anteriores. Uno de sus pasos es la reacción en cadena de la polimerasa (PCR, por sus siglas en inglés).
Esta es una técnica por la que se induce a los genes a replicarse tal como hacen en la naturaleza, pero de forma muy acelerada. Requiere de tiempo, de temperatura precisa y controlada y de ‘alimento’ para los genes, los reactivos adecuados. Además, solo existen métodos operativos y comerciales de replicar genes parecidos a los humanos (ADN), por lo que se necesita convertir los genes (ARN) del virus en ADN antes de poder utilizarla.
Una de las ventajas de la técnica PCR es que está establecida y comercializada por multitud de compañías y se adapta a nuevos virus de forma muy rápida, en días, dado el nivel tecnológico existente y la gran cantidad de diferentes reactivos ya existentes. Además, puede detectar por separado diferentes virus de manera muy precisa y funciona incluso en cantidades muy pequeñas de virus.
Entre sus inconvenientes está la necesidad de instrumentos complejos, precisos y caros para su utilización, por lo que deben centralizarse las muestras en laboratorios con personal especializado, también para saber manejarlos de forma fiable y seguir el proceso de manera muy estricta, ya que, al ser tan sensible, es muy vulnerable a la contaminación. Asimismo, tarda horas en obtener resultados, a las que se añade el tiempo de transportar las muestras al laboratorio y devolver los resultados. Todo esto supone un coste relativamente elevado.
Existen varias técnicas alternativas que permiten detectar los genes del virus de otras formas, pero ninguna de ellas está suficientemente desarrollada como para desplegarla ahora mismo en hospitales y poder usarla para tomar decisiones. Además, muchas de estas nuevas técnicas solo pueden utilizarse con instrumentos que no se fabrican en serie de momento. Por lo tanto, para detectar de forma fiable y operativa los genes del virus en estos momentos solo existe la técnica PCR.
2. Detección del virus como entidad individual (test de antígenos)
En este caso, se detecta el virus entero mediante el uso de anticuerpos dirigidos a interaccionar con unas moléculas, los antígenos (proteínas), presentes en la cubierta del virus, que son bastante específicas y en principio se pueden detectar.
Es una labor ardua de investigación encontrar reactivos, que en realidad son análogos a los anticuerpos que generaría el enfermo que actúen frente a las proteínas específicas de un virus y no frente a otras presentes en la saliva, en las células humanas, en otras bacterias normales o en otros virus. Al ser el coronavirus actual tan parecido al virus que llamamos el SARS, hay algunos reactivos ya desarrollados para esa ocasión que pueden ser utilizados en el momento actual.
Estos métodos se basan en el cambio de color de los reactivos al encontrar virus, por la reacción que se produce con sus proteínas de la cubierta. Por tanto, es necesario que haya una cantidad importante de virus en la muestra para ser efectivos. Al no haber una fase de amplificación de varias horas, estos test son rápidos, produciendo resultados en minutos.
Esta es una de sus innegables ventajas: es una técnica muy rápida, que permite una producción masiva y bajo coste. Además, permite obtener el resultado en el lugar de la muestra y no requiere de personal especializado, aunque sí cuidado en el manejo de la muestra. En principio, detecta la enfermedad desde el primer día siempre que haya cantidad suficiente de virus.
Sin embargo, se encuentra con importantes dificultades: necesita cantidad suficiente de virus en la muestra, por lo que tiene el potencial de dar negativo aun cuando exista la enfermedad y, además, los reactivos deben ser muy específicos y es necesario por tanto tener unos controles de calidad exhaustivos para asegurar la misma calidad (fiabilidad) de lote a lote de fabricación.
3. Detección de anticuerpos en el organismo infectado (test serológico)
Una vez la infección está en marcha, se generan suficientes cantidades de anticuerpos como para poder detectarlos. De hecho, por regla general se conservan los anticuerpos por un tiempo, o para toda la vida, después de superar la infección, lo que confiere inmunidad. Este es el efecto que pretende alcanzar la vacuna sin pasar la enfermedad.
Los anticuerpos están en la sangre, concreta-mente en el suero, y por eso se llaman tests serológicos. Para detectarlos, se utilizan reactivos que contienen partes semejantes a los antígenos, es decir, contrario a los otros test anteriores.
La realización de estas pruebas es muy sencilla, a través de una pequeña muestra de sangre, y el resultado se obtiene muy rápido, entre 5 y 15 minutos. Es una técnica que permite producción masiva a bajo coste; también es portátil, es decir, se obtiene el resultado en el lugar de la muestra sin necesidad de personal especializado, y ya está establecida para otros tipos de uso o para otros virus.
Sus desventajas son que necesita una cantidad suficiente de anticuerpos en la muestra, por lo que existe la posibilidad de que dé negativo aun cuando exista la enfermedad, y que no detecta la enfermedad si acaba de iniciarse, ya que los anticuerpos tardan varios días en generarse según la persona y su estado de salud.




















